2022年10月,爱渡医疗正式推出免疫组化法检测Claudin18.2蛋白表达的检测产品,“产品优、患者广、趋势好、疗效佳、指南入”5大特色,助力推动Claudin18.2靶点新药临床试验的开展。
初次介绍Claudin18.2,很多医生或患者会问:
Claudin18.2作为一个泛癌种的靶点,在多种上皮肿瘤中都有异常表达,已成为热门靶点之一,国内外靶向Claudin18.2靶点的技术路线几乎囊括了所有主流方向:单克隆抗体、双特异性抗体、CAR-T以及ADC。Claudin18.2被寄予厚望,有望成为下一个“PD-1”。
产品优——采用高品质抗体,检测结果稳定准确
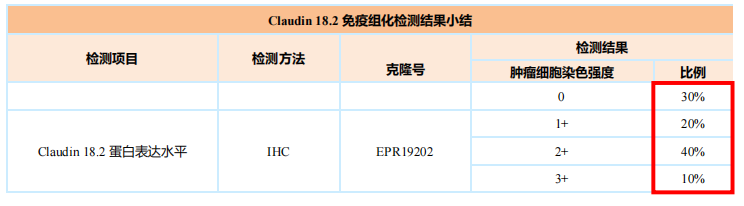
本产品Claudin18.2的检测采用质控严格、信号强、染色稳定的高品质抗体,有效保证染色结果。克隆号为EPR19202,具有高特异性、高灵敏度和高批间稳定性等优势。检测结果分别呈现染色强度和阳性细胞的比例,可以满足目前绝大多数Claudin18.2检测结果的要求,而且与中心实验室复测的结果保持高度一致。
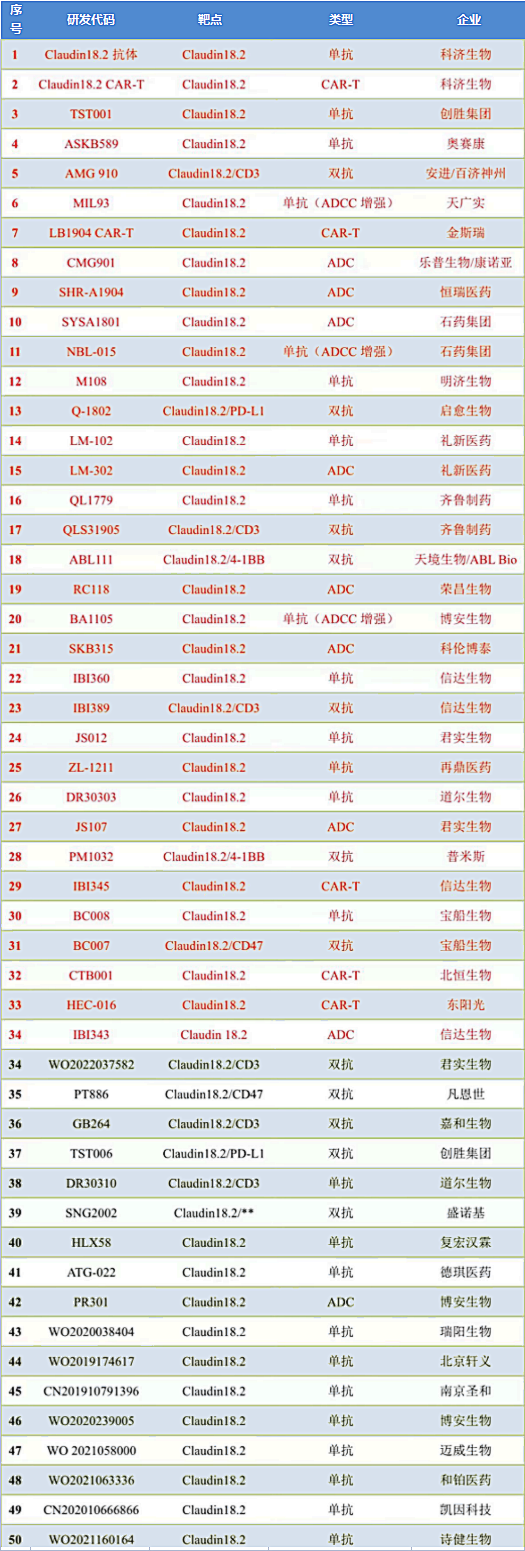
趋势好——国内外竞争激烈,几十款Claudin18.2靶向药物争相亮相!
目前,国内外没有Claudin18.2的靶向药物获批上市。但全球Claudin18.2(CLDN18.2)相关的临床研究近百项,涉及实体瘤、胃和胃食管交界腺癌、胰腺癌、胆道肿瘤、肺癌、食管癌等。国内相关临床试验至少30项,涉及实体瘤、胃和胃食管交界腺癌、胰腺癌等;其中,安斯泰来的Zolbetuximab(佐妥昔单抗)率先进入III期临床试验。多家药企争相布局,足以见得Claudin18.2是一个潜力巨大的靶点。
患者广——覆盖人群广,Claudin18.2蛋白在多种实体瘤中异常表达
Claudin 蛋白是紧密连接分子,主要在上皮细胞中表达,它的功能主要是调节屏障结构的渗透性。已有研究表明,Claudin 蛋白表达的改变会导致紧密连接功能受损,影响信号传导途径,并在某些上皮癌中起到促肿瘤作用。
Claudin18.2是claudin家族的一员,是存在于上皮和内皮紧密连接中的整合素膜蛋白,在多种肿瘤组织中高度表达,比如胃癌(60%~80%)、胰腺癌(50%)、食管癌(30%~50%)和肺癌(40%~60%)等,但是在正常组织中几乎没有表达,因而具有出色的治疗潜力。
疗效佳——疗效可期,Claudin18.2靶向药物延长患者生存期
纵观既往数据,靶向Claudin18.2的药物或疗法取得了显著的疗效,可谓是异彩纷呈。
CT041:靶向Claudin18.2的CART细胞疗法
其I期临床研究纳入了经免疫组织化学证实的肿瘤组织表达 CLDN18.2且接受过至少一种治疗的晚期消化系统癌症患者,共37名患者被纳入本次中期分析,其中 28 名患者为胃或胃食管结合部(GC/GEJ)肿瘤,5 名为胰腺癌(PC),4 名为其他类型消化系统肿瘤。
37 名患者中有 36 名有可测量的靶病灶;其中,30 例(83.3%)患者出现肿瘤消退。本研究总体缓解率(ORR)和疾病控制率(DCR)分别达到 48.6% 和 73.0%,所有患者的中位无进展生存期(mPFS)为 3.7 个月,6 个月时的总生存期(OS)率为 80.1%。胃癌患者的 ORR 和 DCR 分别达到 57.1% 和 75.0%,mPFS 为 4.2 个月,6 个月总生存率为 81.2%。
安全性和耐受性方面,在剂量递增/递减阶段,首次输注后 28 天内未观察到预定义的剂量限制毒性,所有患者都经历了3级或更高的血液学毒性,主要为淋巴细胞绝对值减少。94.6% 的患者出现 1 级或 2 级细胞因子释放综合征(CRS),未报告3级或更高级别的 CRS 或神经毒性、治疗相关死亡或剂量限制性毒性。
此前,CT041被美国FDA授予“再生医学先进疗法”(RMAT)资格,此次在后线胃癌患者中取得的疗效远远优于标准疗法。
Zolbetuximab:全球首款靶向Claudin18.2的单抗
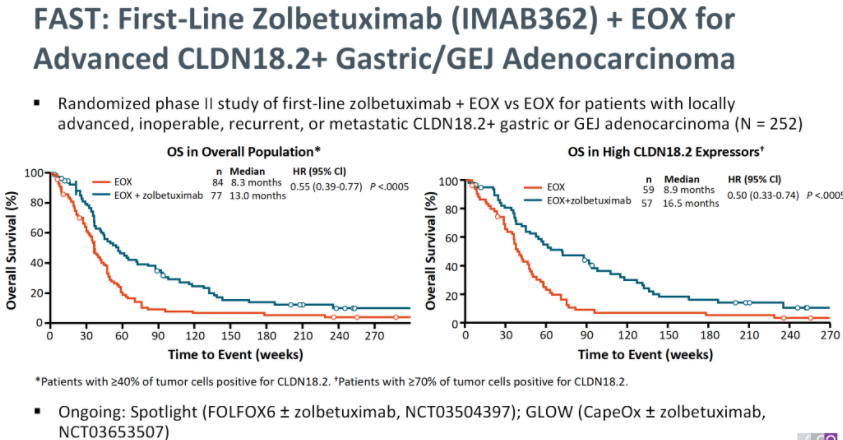
Zolbetuximab是进展最快的单克隆抗体,目前已进入III期临床研究。II期研究评估了Zolbetuximab一线与表柔比星、奥沙利铂和卡培他滨(EOX)化疗对晚期/复发性胃癌/GEJ患者的疗效,纳入CLDN18.2阳性患者。FAST研究显示,实验组和对照组的mPFS分别为7.5个月和5.3个月(危险比(HR)=0.44)。Zolbetuximab联合EOX组OS获益为13.2个月,而单用EOX组为8.4个月(HR=0.56),ORR更高(39%对25%;P=0.022)。mPFS显著延长,尤其是在Claudin 18.2表达比例≥70%的患者中,mPFS为9.0个月vs 5.7个月,mOS为16.5个月vs 8.9个月。
TST001:一种高亲和力的靶向Claudin18.2的单抗
TST001通过抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)机制杀死表达Claudin18.2的肿瘤细胞,具有增强的ADCC和CDC活性,在异种移植试验中显示出强大的抗肿瘤活性。
TST001联合卡培他滨和奥沙利铂(CAPOX)作为晚期胃癌/胃食管连接部癌一线治疗的I期临床研究,截至2022年4月5日,14名患者在剂量递增阶段按每3周1、3、6或8 mg/kg的剂量;12名患者在扩展阶段按每3周6 mg/kg的剂量接受TST001和CAPOX的联合治疗。
在剂量递增阶段并无进行Claudin18.2筛选的9名受试者(有可测量病变且至少接受过一次治疗后肿瘤评估)当中,5名实现部分缓解及3名实现病情稳定,为最佳总体缓解率。
安全性方面,无受试者出现剂量限制性毒性。治疗期间出现的不良事件(TEAEs)大多为1-2级,包括恶心、低白蛋白血症、贫血、呕吐及AST升高。
TST001在表达Claudin18.2的未接受治疗胃癌患者中显示出可控的安全性及令人鼓舞的抗肿瘤活性。
CSCO指南是国内肿瘤诊治最权威的指南之一。2022年CSCO胃癌诊疗指南,三线免疫治疗以注释形式纳入Claudin18.2 CAR-T细胞免疫治疗,为胃癌患者提供了新的选择,也带来了相较于现有的二线标准治疗更好的生存获益。
随着Claudin18.2靶点的深入研究,相信会有越来越多的Claudin18.2靶向药物获批上市,Claudin18.2的检测将会更加重要。提前获取Claudin18.2的表达状态,为参加相关临床试验尽早用上新型靶向药物做好充分的准备,同时也意味着有更多的选择和机会。
在线报名